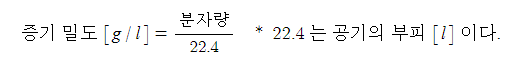1. 위험물
가. 제1류 위험물
|
위험물
|
지정수량
|
|||||
|
유별
|
성질
|
품명
|
화학식
|
|||
|
제1류
|
산화성고체
|
1. 아염소산염류
|
NaClO2
|
50 ㎏
|
||
|
2. 염소산염류
|
NaClO3
|
50 ㎏
|
||||
|
3. 과염소산염류
|
KClO4
|
50 ㎏
|
||||
|
NaClO2
|
||||||
|
4. 무기과산화물
|
K2O2
|
50 ㎏
|
||||
|
Na2O2
|
||||||
|
MgO2
|
||||||
|
5. 브로민산염류
|
NH4BrO3
|
300 ㎏
|
||||
|
6. 질산염류
|
KNO3
|
300 ㎏
|
||||
|
NaNO3
|
||||||
|
NH4NO3
|
||||||
|
AgNO3
|
||||||
|
7. 아이오딘산염류
|
KIO3
|
300 ㎏
|
||||
|
8. 과망가니즈산염류
|
KMnO4
|
1,000 ㎏
|
||||
|
9. 다이크로뮴산염류
|
K2Cr2O7
|
1,000 ㎏
|
||||
|
10. 그 밖에 행정안전부령으로 정하는 것
11. 제1호부터 제10호까지의 어느 하나에 해당하는
위험물을 하나 이상 함유한 것
|
50 ㎏, 300 ㎏
또는 1,000 ㎏
|
|||||
※ 암기법 : 무아과염 아브질, 과중과 : 5, 3, 천
▣ 그밖에 행정안전부령으로 정하는 것
|
위험등급
|
품명
|
지정수량
|
명칭
|
화학식
|
|
|
Ⅰ
|
그외
|
차아염소산염류
|
50 ㎏
|
|
|
|
Ⅱ
|
과아이오딘산
|
300 ㎏
|
|
|
|
|
Ⅱ
|
과아이오딘산염류
|
300 ㎏
|
|
|
|
|
Ⅱ
|
아질산염류
|
300 ㎏
|
|
|
|
|
Ⅱ
|
크로뮴,납,요오드의 산화물
|
300 ㎏
|
삼산화크로뮴
|
CrO3
|
|
|
Ⅱ
|
퍼옥소붕산염류
|
300 ㎏
|
|
|
|
|
Ⅱ
|
퍼옥소이황산염류
|
300 ㎏
|
|
|
|
|
Ⅱ
|
염소화아이소시아눌산
|
300 ㎏
|
|
|
|
▣ 일반적 성질
⊙ 무색 또는 백색의 분말 (고체)이다.
⊙ 불연성, 조연성, 강산화재, 조해성이 있다.
⊙ 비중이 1보다 크다.
⊙ 분자내에 산소를 함유하고 있어, 분해시 산소를 발생한다.
⊙ 폭약의 원료가 된다.
▣ 위험성
⊙ 가연물과 혼합시 연소 또는 폭발의 위험이 있다.
⊙ 가열, 충격, 마찰 등에 의해 분해될 수 있다.
⊙ 알칼리금속의 과산화물은 물과 반응하여 산소를 발생하며 발열한다.
▣ 저장 및 취급
⊙ 가연물과 접촉 및 혼합을 피한다.
⊙ 서늘하고 환기가 잘 되는 곳에 보관한다.
⊙ 알칼리금속의 과산화물은 물과 접촉을 피한다.
▣ 산화성액체 시험방법 및 판정기준 (제1류 위험물)
⊙ 목분(수지분이 적은 삼에 가까운 재료로 하고 크기는 500㎛의 체를 통과하고 250㎛의 체를 통과하지 않는 것).
질산 90% 수용액 및 시험물품을 사용하여 온도 20℃, 습도 50%, 1기압의 실내에서 제2항 및 제3항의 방법에 의하여
실시한다. 다만, 배기를 행하는 경우에는 바람의 흐름과 평행하게 측정한 풍속이 0.5m/s 이하이어야 한다.
⊙ 질산 90% 수용액에 관한 시험순서는 다음 각호와 같다.
- 외경 120㎜의 평저증발접시[화학분석용 자기증발접시 (KS L 1561)] 위에 목분 (온도 105℃에서 4시간 건조하고 건조
용 실리카겔을 넣은 데시케이터 속에 온도 20℃로 24시간 이상 보존되어 있는 것) 15g을 높이와 바닥면의 직경의
비가 1 : 1.75가 되도록 원추형으로 만들어 1시간 둘 것
⊙ 5회 이상의 측정에서 1회 이상의 연소시간이 평균치에서 ± 50%의 범위에 들어가지 않는 경우에는 5회 이상의 측정결
과가 그 범위에 들어가게 될 때까지 제1호 내지 제5호의 조작을 반복할 것
⊙ 시험물품에 관한 시험순서는 다음 각 호와 같다.
- 외경 120㎜ 및 외경 80㎜ 의 평저증발접시의 위에 목분 15g 및 6g 을 높이와 바닥면의 직경의 비가 1 : 1.75가 되도록
원추형으로 만들어 1시간 둘 것
- 제1호의 목분 15g 및 6g의 원추형의 모양에 각각 시험물품 15g 및 24g을 주사기로 상부에서 균일하게 주사하여 목분
과 혼합할 것
⊙ 제2호의 각각의 혼합물에 대하여 제2항제3호 내지 제6호와 같은 순서로 실시할 것. 이 경우 착화 후에 소염하여 훈염
또는 발연상태로 목분의 탄화가 진행하는 경우 또는 측정종료 후에 원추형의 모양의 내부 또는 착화위치의 위쪽에
목분이 연소하지 않고 잔존하는 경우에는 제2항제1호 내지 제4호와 같은 조작을 5회 이상 반복하고, 총 10회 이상의
측정에서 측정횟수의 1/2 이상이 연소할 경우에는 그 연소 시간의 평균치를 연소시간으로 하고, 총 10회 이상의 측정
에서 측정회수의 1/2 미만이 연소한 경우에는 연소시간이 없는 것으로 한다.
- 시험물품과 목분과의 혼합물의 연소시간은 제3호에서 측정된 연소시간 중 짧은 쪽의 연소시간으로 할 것
⊙ 시험물품과 목분과의 혼합물의 연소시간이 표준물질 (질산 90% 수용액)과 목분과의 혼합물의 연소시간 이하인 경우
에는 산화성액체에 해당하는 것으로 한다.
※ 산화성액체 시험방법 : 목분, 질산 90% 수용액을 사용
나. 제2류 위험물
▣ 백(100㎏) 황적, 오(500㎏)철마분, 인고천(1,000㎏)
|
위험물
|
지정수량
|
|||
|
유별
|
성질
|
품명
|
화학식
|
|
|
제2류
|
가연성고체
|
1. 황화인
|
P4S3
|
100 ㎏
|
|
P2S5
|
||||
|
P4S7
|
||||
|
2. 적린
|
P
|
100 ㎏
|
||
|
3. 황
|
S
|
100 ㎏
|
||
|
4. 철분
|
Fe
|
500 ㎏
|
||
|
5. 금속분
|
|
500 ㎏
|
||
|
6. 마그네슘
|
Mg
|
500 ㎏
|
||
|
7. 그 밖에 행정안전부령으로 정하는 것
8. 제1호부터 제7호까지의 어느 하나에 해당하는 위험물을
하나 이상 함유한 것 |
100 ㎏ 또는
500 ㎏
|
|||
|
9. 인화성고체
|
1,000 ㎏
|
|||
<참고>
▣ 인화성 고체 : 인화성 고체라 함은 고형알코올 그 밖에 1기압에서 인화점이 40℃ 미만인 고체를 말한다.
▣ 황린과 적린
P4 (황린) → (260℃ 가열) P4 (적린)
⊙ 황린을 공기를 차단한 상태에서 260℃로 가열하면 적린이 된다.
▣ 위험물이 되는 기준
⊙ 황 : 순도 60wt%이상인 것. 불순물은 활석 등 불연성 물질과 수분에 한한다.
⊙ 철분 : 53㎛의 체를 통과하는 것이 50wt% 이상인 것
⊙ 금속분 : 구리분, 니첼분을 제외하고 150㎛의 체를 통과하는 것이 50wt% 이상인 것
⊙ 마그네슘 : 지름 2㎜ 이상의 막대모양 제외, 2㎜의 체를 통과하지 않는 것 제외
= 지름 2㎜ 미만의 마그네슘은 위험물에 해당한다.
가. 일반적 성질
① 대부분 비중이 1 보다 크거 물에 녹지 않는다.
② 연소가 잘 된다. 산소와 결합이 쉽다. (환원성)
③ 대부분 무기화합물이다.
나. 위험성
① 강산화성 물질과 충격 등에 의하여 폭발할 가능성이 있다.
② 금속분, 철분은 밀폐된 공간 내에서 분진폭발의 위험이 있다. (분진폭발 : 가볍고 작다)
③ 금속분, 철분, 마그네슘은 물, 습기, 산과 접촉하여 수소를 발생하여 발열한다.
다. 저장 및 취급
① 점화원으로 부터 멀리하고 가열을 피할 것 (화기주의)
② 금속분, 철분, 마그네슘은 물, 습기, 산과의 접촉을 피할 것 (화기주의, 물기엄금)
③ 강산화성 물질과의 접촉을 피할 것
#산화성고체 #가연성고체 #강산화성 #환원제 #산화제 #위험물 #염소산염류 #화기주의 #물기엄금 #화기엄금 #점화원 #황린 #적린 #황 #인
'위험물 기능장 실기' 카테고리의 다른 글
| 연소와 소화 (0) | 2025.02.10 |
|---|---|
| 위험물의 종류와 소화설비 (5) | 2025.02.09 |
| 제3류 및 제4류 위험물 (0) | 2025.02.08 |
| 위험물의 종류와 지정수량 (2) | 2025.02.04 |
| 옥내저장소 위치 · 구조 및 시설기준 (0) | 2025.02.03 |