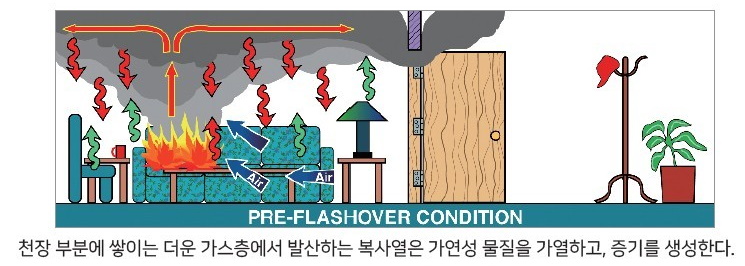
1. 플래시 오버 (Flash over) : 순발 연소
가. 정의
① 폭발적인 착화 현상
② 폭발적인 화재 확대 현상
③ 건물 화재에서 발생한 가연성 가스가 일시에 인화하여 화염이 충만하는 단계
④ 실내의 가연물이 연소됨에 따라 생성되는 가연성 가스가 실내에 누적되어 폭발적으로
연소하여 실 전체가 순간적으로 불길에 휩싸이는 현상
⑤ 옥내 화재가 서서히 진행하여 열이 축적되었다가 일시에 화염이 크게 발생하는 상태
⑥ 다량의 가연성 가스가 동시에 연소되면서 급격한 온도상승을 유발하는 현상
나. 발생시간 : 화재발생 후 5 ~ 6 분 경
다. 발생시점 : 성장기 ~ 최성기 (성장기에서 최성기로 넘어가는 분기점)
라. 실내 온도 : 약 800 ~ 900 [℃]
※ 플래시 오버 포인트 (Flash Over Point) : 내화 건축물에서 최성기로 보는 시점
나. 플래시 오버에 영향을 미치는 것
① 개구율
② 내장재료 (내장 재료의 제성상, 실내의 내장재료)
③ 화원의 크기
④ 실의 내 표면적 (실의 넓이 · 모양)
⑤ 가연물의 양 · 종류
⑥ 산소의 농도
다. 플래시 오버의 발생시간고가 내장재의 관계
① 벽 보다 천장재가 크게 영향을 받는다.
② 가연재료가 난연재료 보다 빨리 발생한다.
③ 열전도율이 적은 내장재가 빨리 발생한다.
④ 내장재의 두께가 얇은 쪽이 빨리 발생한다.
라. 플래시 오버 시간 (FOT)
① 열의 발생속도가 빠르면 FOT는 짧아진다.
② 개구율이 크면 FOT는 짧아진다.
③ 개구율이 너무 크게 되면 FOT는 길어진다.
④ 실내부의 FOT가 짧은 순서는 천장, 벽, 바닥의 순이다.
⑤ 열전도율이 작은 내장재가 발생시각을 빠르게 한다.
2. 백드래프트 (Back draft)
① 산소의 공급이 원활하지 못한 화재실에 급격히 산소가 공급될 경우 순간적으로 연소하
여 화재가 폭풍을 동반하여 실외로 분출하는 현상
② 소방대가 소방 활동을 위하여 화재실의 문을 개방할 때 신선한 공기가 유입되어 설내에
축적되었던 가연성 가스가 단시간에 폭발적으로 연소함으로써 화재가 폭풍을 동반하여
실외로 분출되는 현상으로 감쇠기에 나타 난다.
③ 화재로 인하여 산소가 부족한 건물 내에 산소가 새로 유입된 때 고열가스의 폭발 또는
급속한 연소가 발생하는 현상
④ 통기력이 좋지 않은 상태에서 연소가 계속되어 산소가 심히 부족한 상태가 되었을 때
개구부를 통하여 산소가 공급되면 실내의 가연성 혼합기가 공급되는 산소의 방향과
반대로 흐르며 급격히 연소하는 현상으로서 "역화현상"이라고 하며 이 때에는 화염이
산소의 공급통로로 분출되는 현상을 눈으로 확인할 수 있다.
※ draft : 미국식 [dræft] 영국식 [drɑːft] 1. [명사] (아직 완성본이 아닌) 원고, 초안 2. [명사][금융] (은행이 발행한) 어음
3. [형용사][美] (== draught) 기사의 초고
1. [명사] (방 안 같은 한정된 공간 안에 흐르는 한 줄기의) 찬바람[외풍]
2. [명사][격식] 죽 들이마시기, 한 모금, 3. [형용사] (병이 아니라) 통에서 따라 파는
4. [형용사][격식] 무거운 짐을 끄는 데 쓰는
bank draft (banker's draft) 미국식 영국식 [명사] 은행 환어음
draft dodger 미국식 영국식 [명사][美 못마땅함] 병역 기피자 (→conscientious objector
Draft MLB 2012 : [스포츠] 2012년 메이저 리그 신인 선수 선택 회의
【 출제 예상 문제】
1. 플래시 오버 (Flash over)에 대한 설명으로 옳은 것은 ? ②
① 건물화재에서 가연물이 착화하여 연소하기 시작하는 단계이다.
② 축적된 가연성 가스가 일시에 인화하여 화염이 확대되는 단계이다.
③ 건물화재에서 화재가 쇠퇴기에 이른 단계이다.
④ 건물화재에서 가연물의 연소가 끝난 단계이다.
[플래시 오버] 화재실 내 열분해에 의해 축적된 가연성 가스에 의해 실 전체에 화염이 확산
되는 현상을 말하는데 국부적인 화재에서 실 전체로의 화재확대를 의미하며, 성장기에
서 최성기로 넘어가는 분기점이 된다.
2. 플래시 오버 (Flash over) 현상에 대한 설명으로 틀린 것은 ? ①
① 산소의 농도와 무관하다.
② 화재공간의 개구율과 관계가 있다.
③ 화재공간 내의 가연물의 양과 관계가 있다.
④ 화재실 내의 가연물의 종류와 관계가 있다.
[플래시 오버에 영향을 미치는 것]
① 개구율 ② 내장재료 (내장 재료의 제성상, 실내의 내장재료)
③ 화원의 크기 ④ 실의 내표면적 (실의 넓이 · 모양)
⑤ 가연물의 양·종류 ⑥ 산소의 농도
3. 일반적으로 화재의 진행 상황 중 플래시 오버는 어느 시기에 발생하는가 ? ②
① 화재발생 초기 ② 성장기에서 최성기로 넘어가는 분기점
③ 최성기에서 감쇠기로 넘어가는 분기점 ④ 감쇠기 이후
[플래시 오버] 화재실 내 열분해에 의해 축적된 가연성 가스에 의해 실 전체로 화염이 확산
되는 현상을 말하는 데 국부적인 화재에서 실 전체로의 화재확대를 의미하며, 성장기에
서 최성기로 넘어가는 분기점이 된다.
4. 화재가 일정 이상 진행되어 문틈으로 연기가 새어들어 오는 화재를 발견할 때의 일반적
인 안전대책으로 잘못된 것은 ? ①
① 빨리 문을 열고 복도로 대피한다.
② 바닥에 엎드려 숨을 짧게 쉬면서 대피대책을 세운다.
③ 문을 열지 않고 수건 등으로 문틈을 완전히 밀폐한 후 창문을 열고 화재를 알린다.
④ 창문으로 가서 외부에 자신의 구원을 요청한다.
[피난] 문틈으로 연기가 들어 올 경우 급하게 문을 열면 화염 내지 연기에 의해 위해를
받을 수 있으며 심할 경우 백드래프트(Back draft)가 일어날 수 있기 때문에 연기가
들어오는 것을 막고 대책을 강구하여 창문 등으로 구원요청을 하여야 한다.
5. 내화건물의 화재에서 백드래프트 (back draft) 현상은 주로 언제 나타나는가 ? ①
① 감쇠기 ② 초기 ③ 성장기 ④ 최성기
[백드래프트(Back draft)] : 소방대가 소방활동을 위하여 화재실의 문을 개방할 때 신선한
공기가 유입되어 실내에 축적되었던 가연성 가스가 단기간에 폭발적으로 연소함으로
써 화재가 폭풍을 동반하며 실외로 분출되는 현상으로 감쇠기에 나타난다.
6. 플래시 오버 (Flash over) 발생시간과 내장재의 관계에 대한 설명 중 틀린 것은 ? ②
① 벽 보다 천장재가 크게 영향을 미친다.
② 난연재료는 가연재료 보다 빨리 발생한다.
③ 열전도율이 작은 내장재가 빨리 발생한다.
④ 내장재의 두께가 얇은 쪽이 빨리 발생한다.
[플래시 오버(Flash over)의 발생시간과 내장재의 관계]
① 벽 보다 천장재가 크게 영향을 받는다.
② 가연재료가 난연재료 보다 빨리 발생한다.
③ 열전도율이 적은 내장재가 빨리 발생한다.
④ 내장재의 두께가 앏은 쪽이 빨리 발생한다.
7. 산소의 공급이 원활하지 못한 화재실에 급격히 산소가 공급될 경우 순간적으로 연소하여
화재가 폭풍을 동반하여 실외로 분출하는 현상은 ? ③
① 플래시 오버 ② 보일오버 ③ 백드래프트 ④ 슬롭오버
[백드래프트 (back draft) ]
① 산소의 공급이 원활하지 못한 화재실에 급격히 산소가 공급될 경우 순간적으로 연소하
여 화재가 폭풍을 동반하여 실외로 분출하는 현상
② 소방대가 소방활동을 위하여 화재실의 문을 개방할 때 신선한 공기가 유입되어 실내에
축적되었던 가연성 가스가 단기간에 폭발적으로 연소함으로써 화재가 폭풍을 동반하
며 실외로 분출되는 현상으로 감소기에 나타난다.
③ 화재로 인하여 산소가 부족한 건물 내에 산소가 새로 유입된 때 고열가스의 폭발 또는
급속한 연소가 발생하는 현상
④ 통기력이 좋지 않은 상태에서 연소가 계속되어 산소가 심히 부족한 상태가 되었을 때
개구부를 통하여 산소가 공급되면 실내의 가연성 혼합기가 공급되는 산소의 방향과
반대로 흐르며 급격히 연소하는 현상으로서 "역화현상"이라고 하며 이 때에는 화염이
산소의 공급 통로로 분출되는 현상을 눈으로 확인할 수 있다.