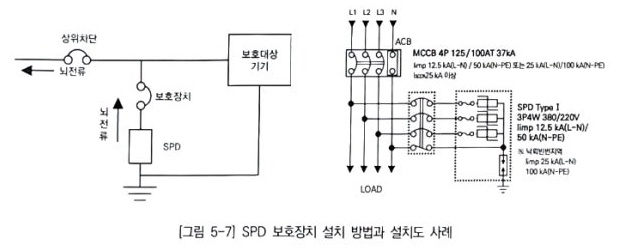
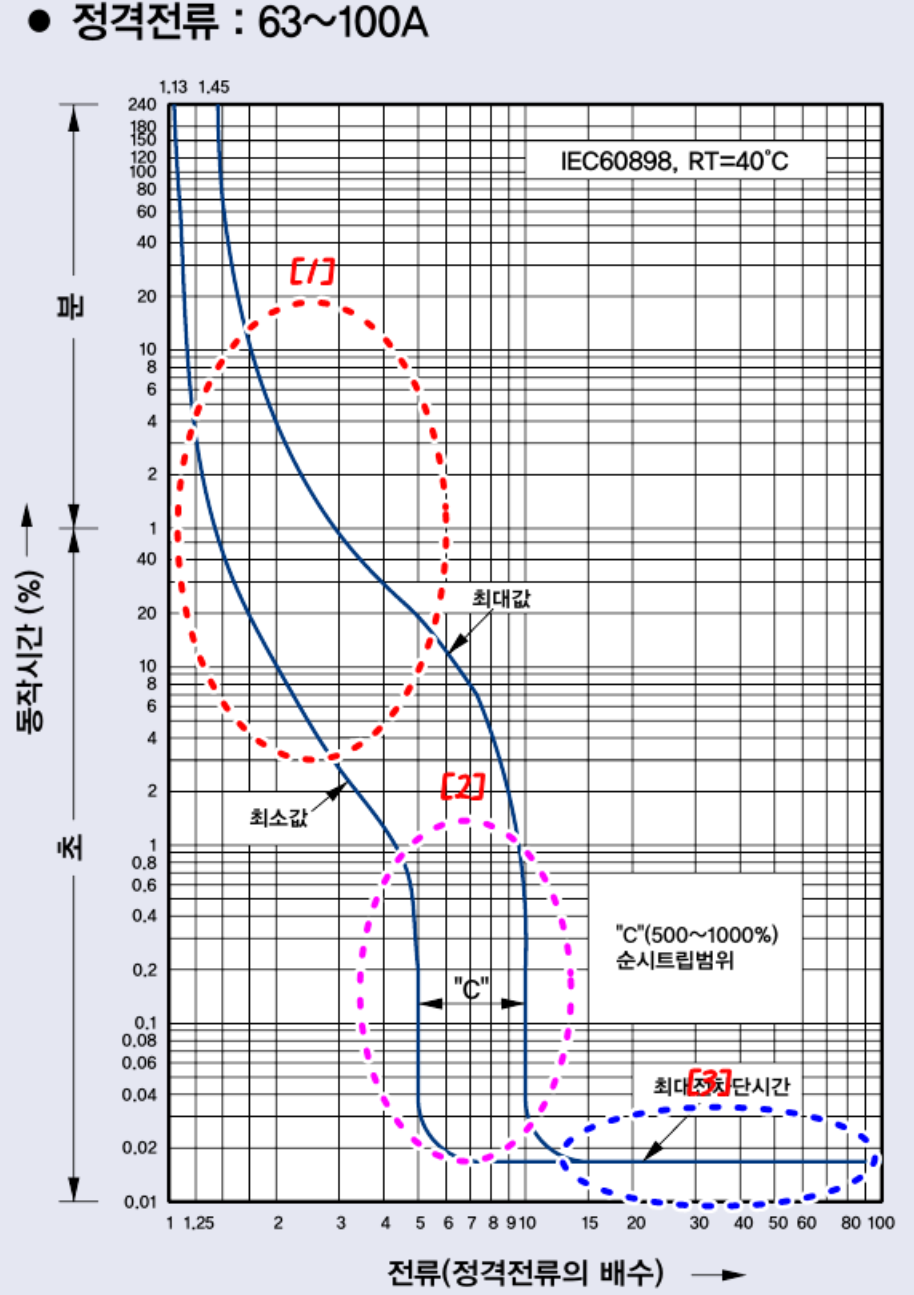
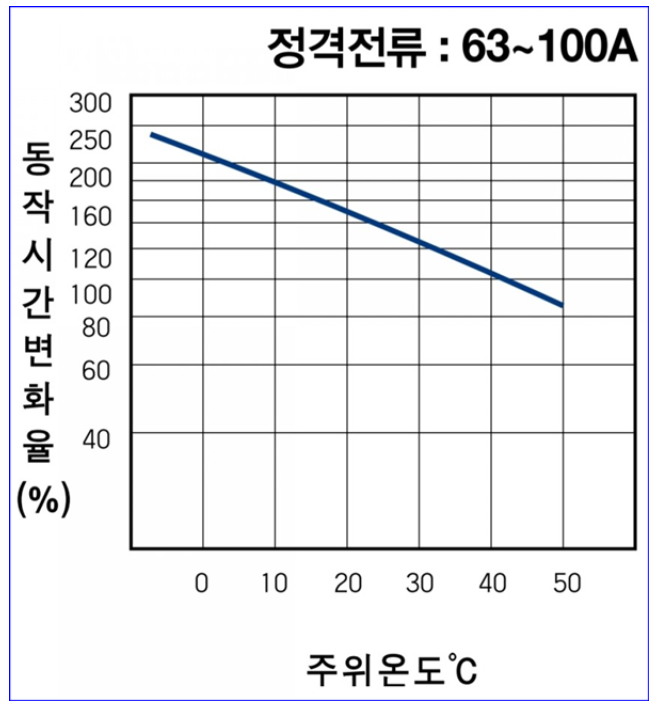
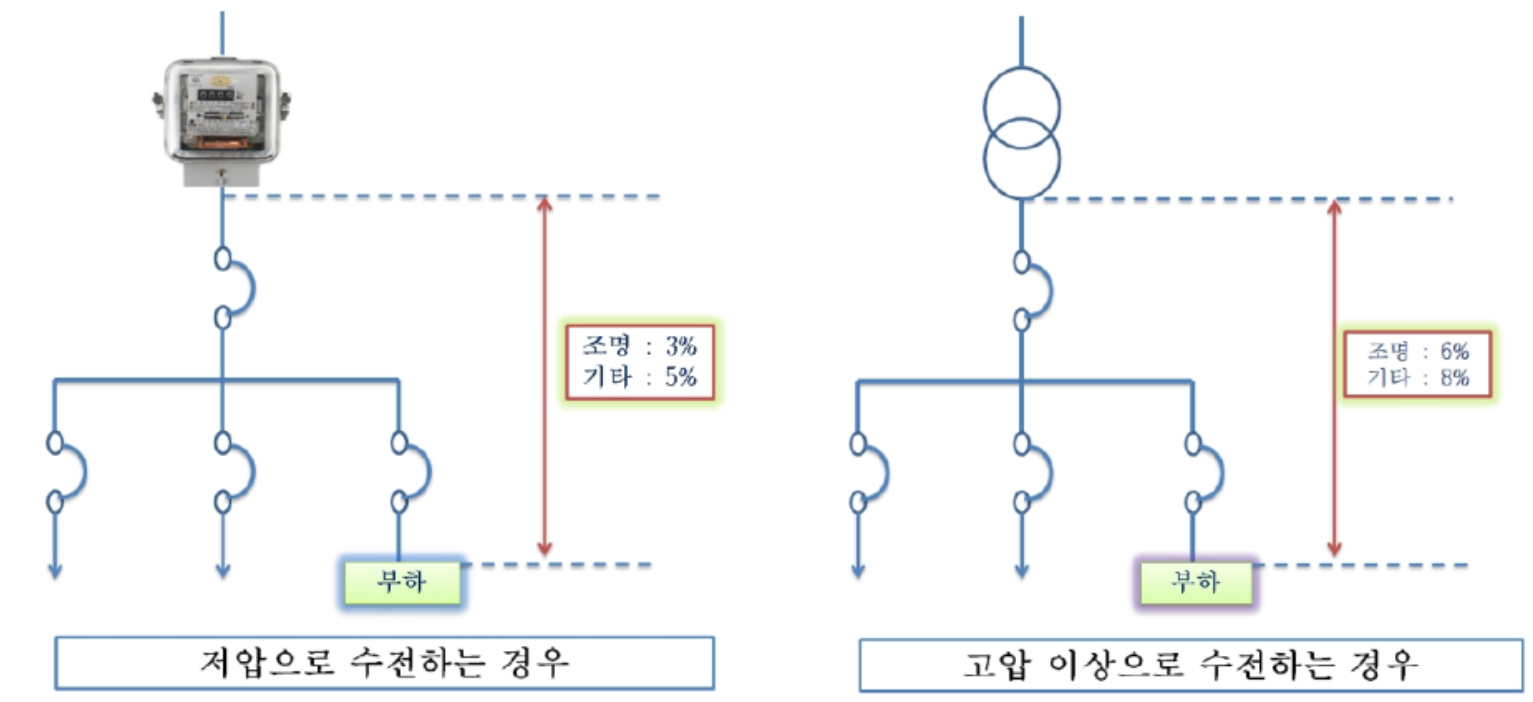
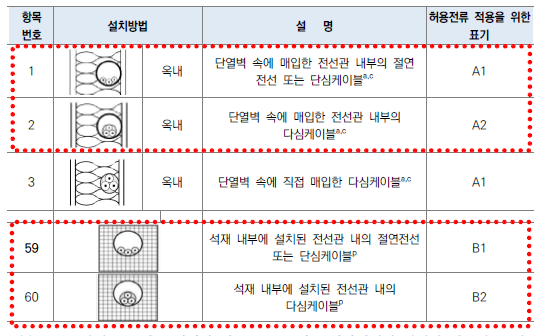
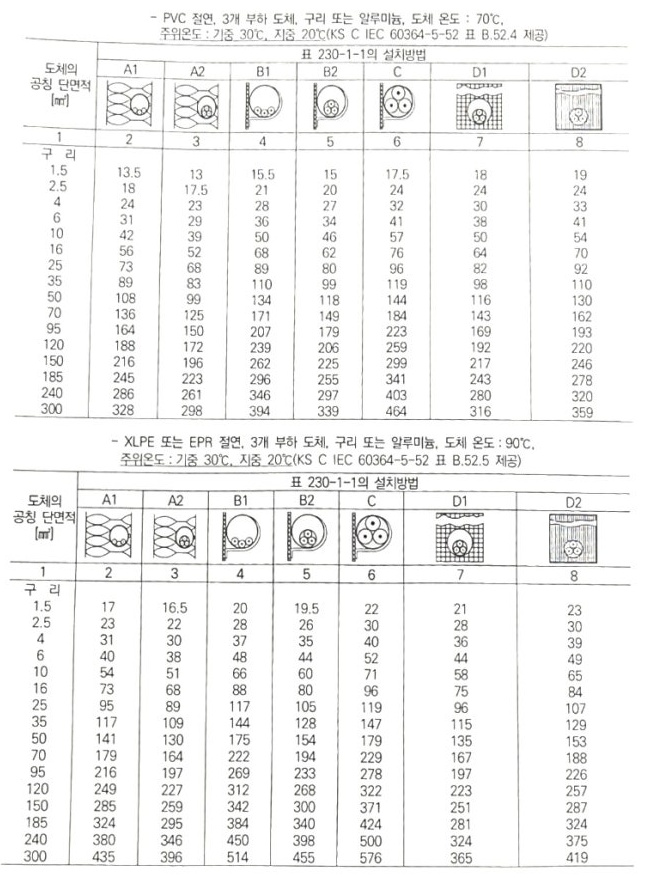
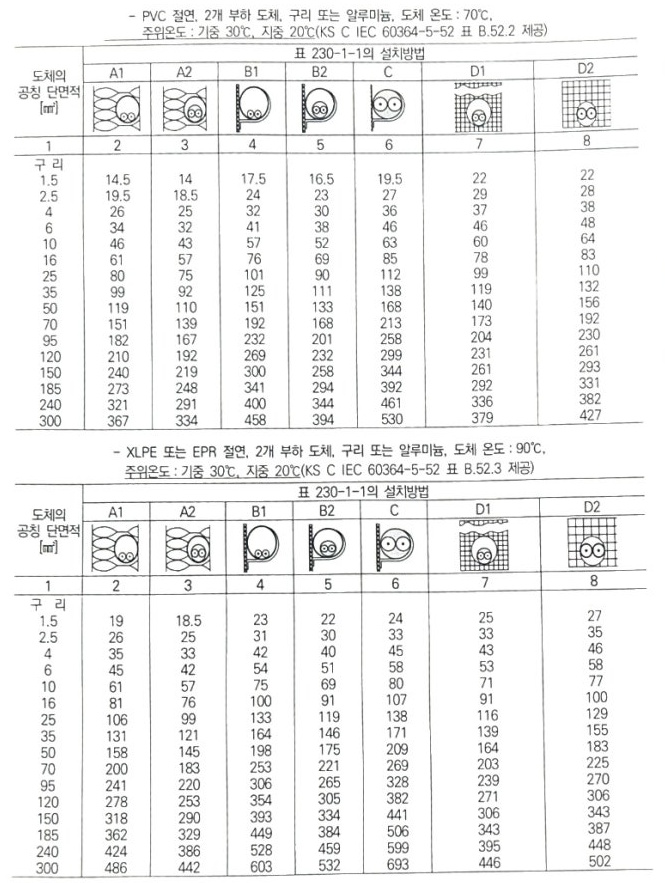
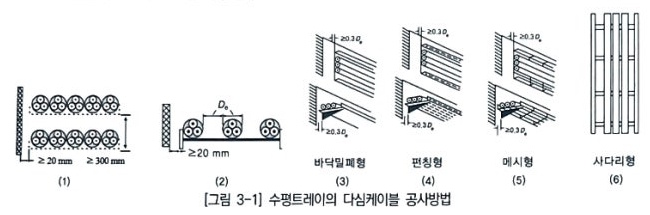
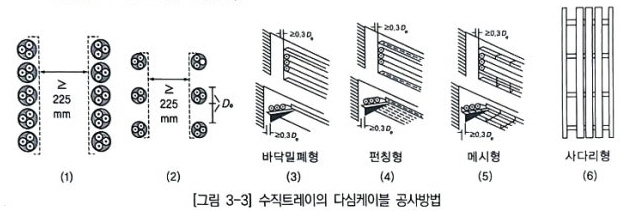
1. 전기설비의 개요
▣ 건축물의 용도가 정해지면 계획단계에서 여러가지 설비로 검토할 필요가 있다.
특히, 현재는 정보화 사회이며 건축물의 추세도 점차 인델리전트화 되어 가고, 이에 대응할 수 있는 전기설비가 요구되어 지고
있으며 고품질의 전력공급을 할 수 있어야 함은 물론, 사고에 의한 정전 파급, 전압 변동 등 다른 수용가에 심한 영향을 주지
않아야 한다.
▣ 전기설비를 계획에 있어
① 안정성
② 설비의 신뢰성
③ 에너지 절감 효과
④ 장래에 대한 융통성, 호환성
⑤ 신기술 도입
⑥ 경제적이면서 간단한 설계
등에 관하여 만족할 만한 계획을 수립하여야 한다.
위와 같은 기능상 문제 이외에도 건축물의 환경을 개선할 수 있는 전기설비를 계획해야 하나, 여기서는 개략적인 부분만 설명하고
더 자세한 자료는 전문서적을 참고한다.
가. 설계의 종류 및 내용
|
계획
|
설비
|
주요내용
|
|
계획설계
|
- 현장조사 및 기본계획
- 설비의 안전성 검토
- 설비의 신뢰성 검토
- 설비의 경제성 검토
- 환경대책 및 취급관리의 편리성 검토
|
|
|
기본 설계
|
전원설비
|
- 부하조사 및 수전용량, 변압기, 뱅크
- 수전, 배전방식 결정
- 예비전원 설비 결정
- 전기실 위치 및 면적 결정
|
|
전력공급설비
|
- 사용전선, 케이블 종류 결정
- 간선의 배선방식 결정
- 간선의 매설방식 결정
- EPS실 면적 확보
|
|
|
전력부하설비
|
- 에너지를 소비하는 설비
(전등, 전열, 동력, 히팅 설비 등)
|
|
|
개략공사비 산출
|
추정 공사비 산출
|
|
|
실시설계
|
전력부하설비
|
- 전등설비
- 전열설비
- 동력설비
- 특수 장소의 전기설비
|
|
전원설비
|
- 수 · 변전설비
- 예비전원설비 (UPS 등)
- 특수전원설비 (신재생에너지 등)
|
|
|
전력 공급설비
|
- 배전방식
- 간선 결정 및 배선
- 분전반 구성
|
|
|
감시제어설비
|
- 조명 제어설비
- 전력 감시 제어설비
|
|
|
반승설비
|
- 엘리베이터 설비
- 에스컬레이터 설비
- 전동 덤웨이터
|
|
|
정보 · 통신설비
|
- 전화설비
- TV 설비
- 인터폰설비
- 뉴미디어 정보설비
- 통합 배선설비
|
|
|
방재설비
|
- 피뢰설비, 접지설비
- 방범설비
- 항공장애 표시등 설비
|
|
2. 수 · 변전설비 계획
가. 수 · 변전설계의 계획 절차
|
계획절차
|
주요 내용
|
|
자료조사
↓
|
⊙ 부하의 종류, 특성, 성능, 운전조건
⊙ 부하용량, 보호 조작방식
⊙ 부하의 위치, 지형조건, 주변환경, 방재상
|
|
부하용량 결정
↓
|
⊙ 전등설비
⊙ 일반 동력부하
⊙ 상용, 예비
⊙ 신재생에너지 등
|
|
수전용량 추정
↓
|
⊙ 부하일람표에 의한 방법
⊙ 실 부하법
|
|
수전방식의 결정
↓
|
⊙ 인입경로 검토
⊙ 공급방안 검토
⊙ 한국전력공사와 협의
⊙ 계약전력 결정
|
|
부하전압 결정
↓
|
⊙ 부하특성 파악
|
|
기본 계획 수립
↓
|
⊙ 수전방식 검토
⊙ 변압기의 Bank수 결정
⊙ 모선구성의 검토
⊙ 접지방식의 검토
⊙ 배전방식의 검토
⊙ 비상전원의 검토
⊙ 감시, 조작의 정도
|
|
주회로조건의 검토
↓
|
⊙ 정격전류
⊙ 단락전류
⊙ 지락전류
⊙ 전압 변동
⊙ 역률 개선
⊙ 절연협조
|
|
주회로 기기의 정격결정
↓
|
⊙ 주회로 조건 검토 후 전기방식 검토
|
|
보호방식의 검토
↓
|
⊙ 계전기 선정
⊙ 보호 협조
|
|
조작 및 감시계통 검토
↓
|
⊙ 유지, 보수, 관리
⊙ 감시, 제어
⊙ 원격 제어
⊙ 전력량 계측
|
|
변전실 검토
↓
|
⊙ 옥내
⊙ 지하
⊙ 옥외
⊙ 주위 환경 (염해, 공해, 소음, 진동 등 고려)
|
|
수전설비 결정
↓
|
⊙ 단선결선도 작성
⊙ 기기 배치도 작성
⊙ 시방서 작성
|
|
검 토
↓
|
⊙ 경제성 검토 (개략 공사비 산출)
|
|
계획 완료
|
|
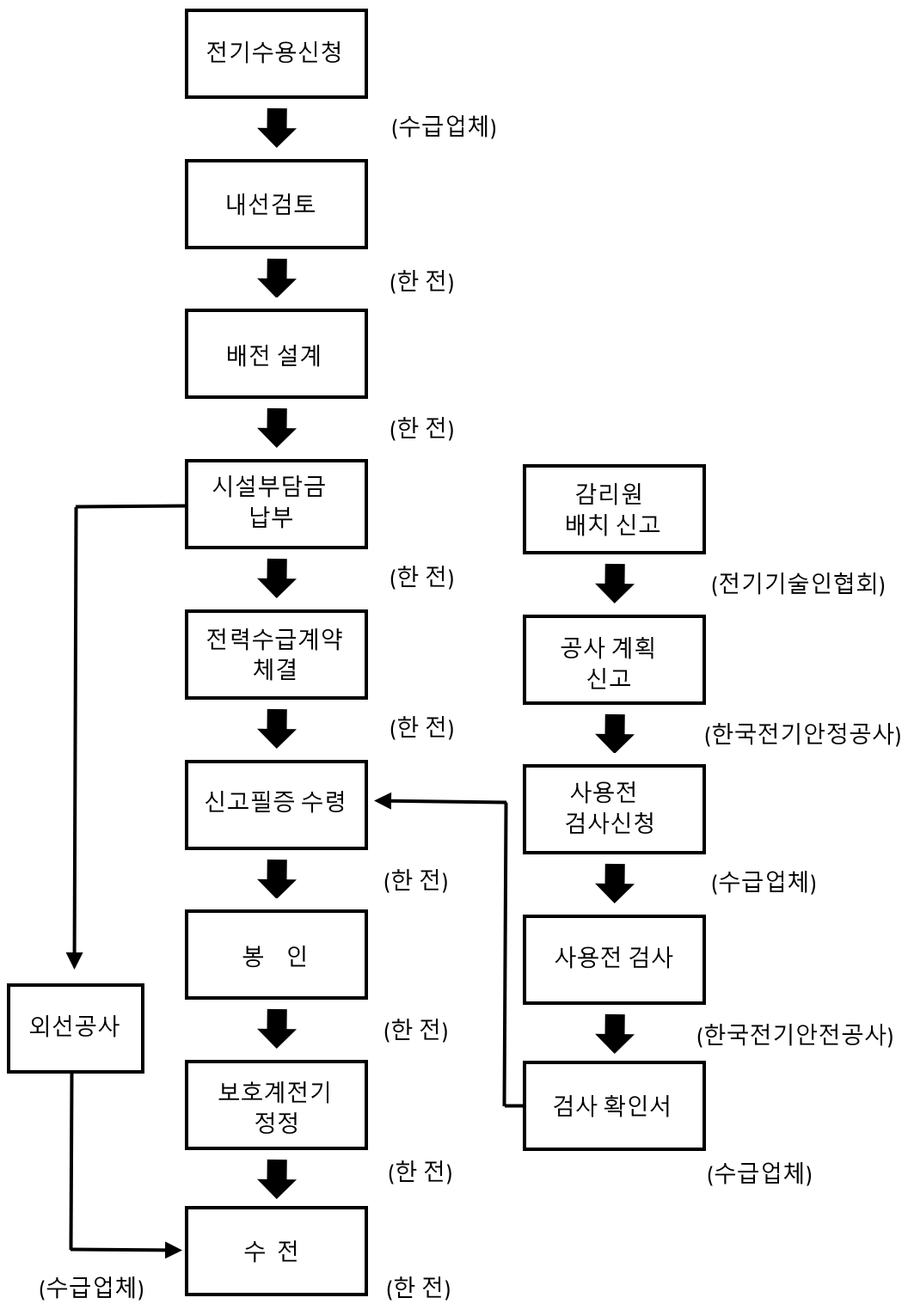
나. 인 · 허가 업무 흐름도
다. 부하의 상정
① 건물 용도별 부하밀도 [VA/㎡]
|
건물별
|
조명
|
일반동력
|
기타동력
|
합 계
|
|
대형 사무실
|
37
|
59
|
37
|
133
|
|
점포 (대형)
|
62
|
72
|
43
|
177
|
|
호 텔
|
38
|
53
|
27
|
118
|
|
주 택
|
28 (51)
|
14
|
28
|
70 (93)
|
|
학 교
|
27
|
15
|
18
|
60
|
|
종합병원
|
47
|
64
|
48
|
159
|
|
체 육 관
|
32
|
34
|
23
|
89
|
|
연 구 소
|
60
|
108
|
53
|
221
|
|
대형 창고
|
18
|
45
|
33
|
96
|
|
대형 전산센타
|
33
|
92
|
60
|
185
|
|
공공건물
|
32
|
41
|
31
|
104
|
② 건물별 표준부하
|
건물명
|
표준부하 [VA/㎡]
|
|
공장, 연회장, 교회, 영화관 등
|
10
|
|
기숙사, 호텔, 목욕탕, 병원, 음식점
|
20
|
|
사무실, 은행, 상점
|
30
|
|
주택, 아파트
|
40
|
③ 건축물 중 별도 계산 할 표준 부하 (공동주택 제외)
|
건축물의 부분
|
표준부하 [VA/㎡]
|
|
복도, 계단, 세면장, 창고, 다락 등
|
5
|
|
강당, 관람석
|
10
|
④ 표준 부하에 따라 산출한 수치에 가산하여야 할 VA수
㉠ 주택, 아파트 (1세대 마다)에 대하여는 500~1,000 [VA]
㉡ 상점의 쇼 윈도우에 대하여는 쇼 윈도우 폭 1m 에 대하여 300 [VA]
㉢ 옥외의 광고등, 전광사인, 네온사인 등의 VA 수
㉣ 극장, 댄스홀 등의 무대조명, 영화관 등의 특수 전등부하의 VA 수
⑤ 수구의 종류에 의한 예상 부하
|
수구의 종류
|
예상부하 (VA/개)
|
|
소형 전등 수구, 콘센트
|
150
|
|
대형 전등 수구
|
300
|
⑥ 공동주택의 용량산정
㉠ 주택건설기준 등에 관한 규정 (제40조)
- 주택의 전기시설용량은 각 세대별 3kW 이상으로 한다.
- 60㎡ 이상인 경우에는 3kW에 60㎡를 초과하는 10㎡ 마다 0.5kW를 더한 값으로 한다.
㉡ (구) 내선규정 (부록)
- P [VA] = 40 VA/㎡ × 바닥면적 [㎡] + (500 ~ 1,000) VA
( )안의 가산 VA는 1,000을 채택하는 것이 바람직하다.
㉢ 전전화(全電化) 주택의 용량산정 : (구)내선규정(부록)
- P [VA] = 60 VA/㎡ × 바닥면적 [㎡] + 4,000 VA
⑦ 근린생활시설의 용량 산정 (표준부하 산정은 전용면적 기준임)
|
구 분
|
일반점포
|
슈퍼마켓
|
|||
|
전등
|
동력
|
냉방
|
계
|
||
|
단위면적당 부하 [VA/㎡]
|
150
|
35
|
95
|
50
|
180
|
⑧ 주요건축물의 수용률 (참고값)
|
종류
구분
|
백화점 · 쇼핑센타
|
사무용 빌딩
|
||
|
범위
|
중앙값
|
범위
|
중앙값
|
|
|
전등 · 전열부하
|
58~92
|
75
|
65~83
|
70
|
|
일반 동력부하
|
47~83
|
65
|
38~72
|
55
|
|
OA 기기 부하
|
-
|
-
|
42~78
|
60
|
|
냉방 동력부하
|
65~95
|
80
|
59~91
|
75
|
|
종류
구분
|
종합병원용 빌딩
|
호텔용 빌딩
|
||
|
범위
|
중앙값
|
범위
|
중앙값
|
|
|
전등 · 전열부하
|
45~75
|
60
|
49~71
|
60
|
|
일반 동력부하
|
40~70
|
55
|
42~68
|
55
|
|
OA 기기 부하
|
45~75
|
60
|
-
|
-
|
|
냉방 동력부하
|
70~100
|
85
|
64~96
|
85
|
#전기설비 #기본설계 #실시설계 #전원설비 #표준부하 #부하밀도 #가산부하
'최신뉴스 > KEC' 카테고리의 다른 글
| 피뢰시스템 (KEC 150) (0) | 2026.04.02 |
|---|---|
| 감전에 대한 보호 (KEC 211) (0) | 2026.03.29 |
| 접지시스템(KEC 140), 계통접지(KEC 203) (0) | 2026.03.25 |
| 과전류 보호와 기기 (KEC 212) (0) | 2026.03.23 |
| 배관규격 결정 (KEC 232.5) (0) | 2026.03.22 |