【 열역학 (Thermodynamics】
▣ 물질의 #상태 변화에 따라 발생하는 열과 일의 양은 열역할 법칙으로 정의되는 에너지와 엔트로피 등의 열역학적
변수들을 이용하여 분석하는 학문
※ 일 ↔ 열 : #물리적 #현상
1. 열역학 제0법칙 [열평형, 온도평형의 법칙]
▣ #온도 가 서로 다른 물체를 접촉시켜 놓으면 얼마 후 온도가 같아진다. (열평형상태)
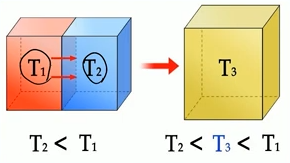
◈ 고온체와 저온체를 함께 놓으면 열이 고온에서 저온으로 이동하여 온도가 같아지려는 성향을 갖는다.
(온도계의 원리)
2. 열역학 제1법칙 : 에너지 보존법칙
▣ 어떤 고립된 계의 총에너지는 일정하다는 법칙
⊙ 내부에너지 변화가 계에 가해진 열과 계가 한일 사이의 차가 같다는 것을 의미한다.
⊙ #에너지 는 생성되지도 소멸되지도 않는다.

◈ 에너지의 양적관계
◈ 열 = 에너지 = 일
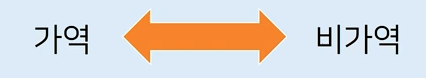
◈ 가역적인 법칙
⊙ 열 ↔ 일, 1[kcal] = 4.184 [kJ]
4.184[kJ/kcal] : 열의 일당량
이를 그림으로 표현하면 다음과 같다.
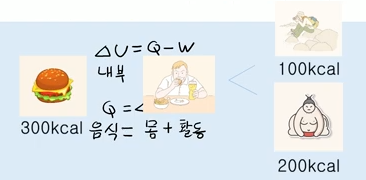
열과 운동의 관계로 정리를 하면..
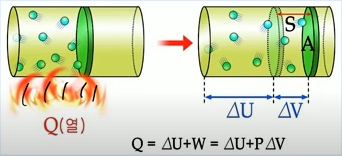
3. 열역학 제2법칙
▣ 고립계에서 총 엔트로피의 변화는 항상 증가하거나 일정하며 절대로 감소하지 않는다.
① 열은 자연적으로 저열원에서 고열원으로 이동할 수 없다.
② #효율 100%의 열기관은 존재할 수 없다.
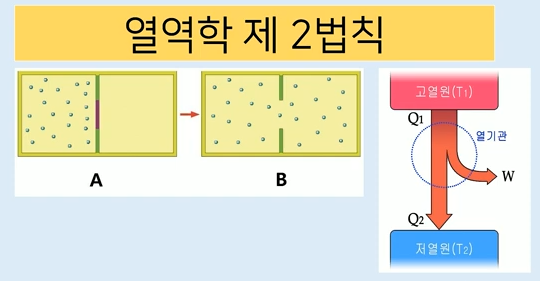
※ 열역학 제2법칙 (에너지 흐름의 법칙)
◈ 자연적 · #경험적 법칙
◈ 일 → #열
◈ #열효율 100 [%]는 없다. * 인위적으로 가야 하므로 효율이 떨어진다.
◈ #비가역적 법칙이다.
4. #열역학 제3법칙
▣ #절대온도 에 가까워질수록 엔트로피의 변화량은 0에 수렴한다.
그리고 계는 절대온도 0도에 이를 수 없다.

|
1종 영구기관 및 2종 영구기관
▣ 1종 영구기관 : 열역학 1법칙에 위배되는 기관
▣ 2종 영구기관 : 열역학 2법칙에 위배되는 기관
|
【 열량의 단위】
◈ 1 [kcal] : 표준 대기압에서 순수한 물 1[㎏]을 1[℃] 올리는데 필요한 열량
◈ 1[btu] : 1파운드의 물을 1[°F] 만큼 올리는데 필요한 열량
◈ 1[CHU] : 1파운드의 물을 1[℃] 올리는데 필요한 열량
섭씨 : 14.5 ⇒ 15.5 [℃] 화씨 : 60 ⇒ 61 [°F]
【 비열 】
◈ 비열이란 어떤 물질의 단위 질량을 1[℃] 만큼 올리는데 필요한 열량
◈ 단위질량을 단위 온도만큼 올리는데 필요한 열량
* 기체의 비열에는 2가지가 있다. : 정합비열과 정적비열로 나뉜다.
⊙ 정합비열 : 압력이 일정할 때 (CP: constant pressure)
⊙ 정적비열 : 체적이 일정할 때 (CP : constant volume)
Cp > Cv
Cp - Cv = R (기체상수)
Cp / Cv > 1
★ #수증기 #비열 0.44 [cal/g ℃]
'소방설비기사 (전기) > 소방원론' 카테고리의 다른 글
| 건축물의 내화성상 및 안전관리 (2) | 2023.04.16 |
|---|---|
| 목재 건축물의 화재 성상 : 소방원론 (0) | 2023.04.15 |
| 전열 · 열전달 현상 : 화재론 (1) | 2023.04.15 |
| 연기 - 화재론 (0) | 2023.04.15 |
| 연소 생성물 (2) | 2023.04.14 |
