▣ 주기율 : 원소를 원자 번호 순으로 나열했을 때 화학적 성질이 비슷한 원소들이 일정한 간격으로 반복되어 나타는 현상
▣ 주기 (period)
⊙ 가로줄
⊙ 1~7주기
⊙ 같은 주기의 원소는 전자껍질수가 같다.
▣ 족 (group)
⊙ 세로줄
⊙ 1~18족
⊙ 같은 족에 속한 원소들은 원자가 전자수가 같다.
⊙ 같은 족에 속한 원소들은 화학적 성질이 비슷하기 때문에 동족 원소라고 한다. (단, 수소제외)
※ 가장 최근에 공식 인정받은 원소까지 포함된 주기율표는 118번까지 포함되어 있는 주기율표이다.
★ 원소의 주기성 : 원소를 원자번호 순서대로 배열하면 일정한 간격을 두고 같은 성질을 지닌 원소가 나타난다.
→ 주기율표의 세로줄에 속하는 같은 족 원소(동족원소)는 화학적 성질이 비슷하다.
① 같은 주기(가로줄)에 있는 원소들은 전자껍질수가 같다.
주기율 표에서는 가로줄을 주기라고 표현하므로 위에서 부터 1주기, 2주기, 3주기가 된다.
⊙ 1주기 (첫번째 가로줄)의 수소(H)와 헬륨(He) → 전자껍질수 1개
⊙ 2주기(두번째 가로줄)의 리튬(Li) ~ 네온(Ne)까지의 원소들 → 전자껍질 2개
⊙ 3주기(세번째 가로줄)의 나트륨(Na) ~ 아르곤(Ar)까지의 원소들 → 전자껍질 3개
② 같은 족(세로줄)에 있는 원소들은 가장 바깥 껍질에 있는 전자의 수가 같다. 즉, 원자가 전자의 수가 같다.
주기율표에서는 세로줄을 족이라고 표현하므로 맨 왼쪽부터 1족, 2족 ··· 17족, 18족이 된다. 또한 가장 바깥껍에 채워져 있는
전자를 원자가 전자라고 한다.
⊙ 1족(맨 왼쪽의 세로줄)의 수소(H), 리튬(Li), 나트륨(Na), 칼륨(K) → 원자가 전자수 1개
⊙ 2족의 베릴륨(Be), 마그네슘(Mg), 칼슘(Ca) → 원자가 전자수 2개
·····
⊙ 17족의 F(플루오린), Cl(염소) → 원자가 전자수 3개
⊙ 18족(마지막 세로줄)에서는 헬륨(He)만 가장 바깥껍질에 채워진 전자의 수가 2개이고 나머지 네온(Ne), 아르곤(Ar) 부터는
가장 바깥 껍질에 8개의 전자가 채워져 있다.

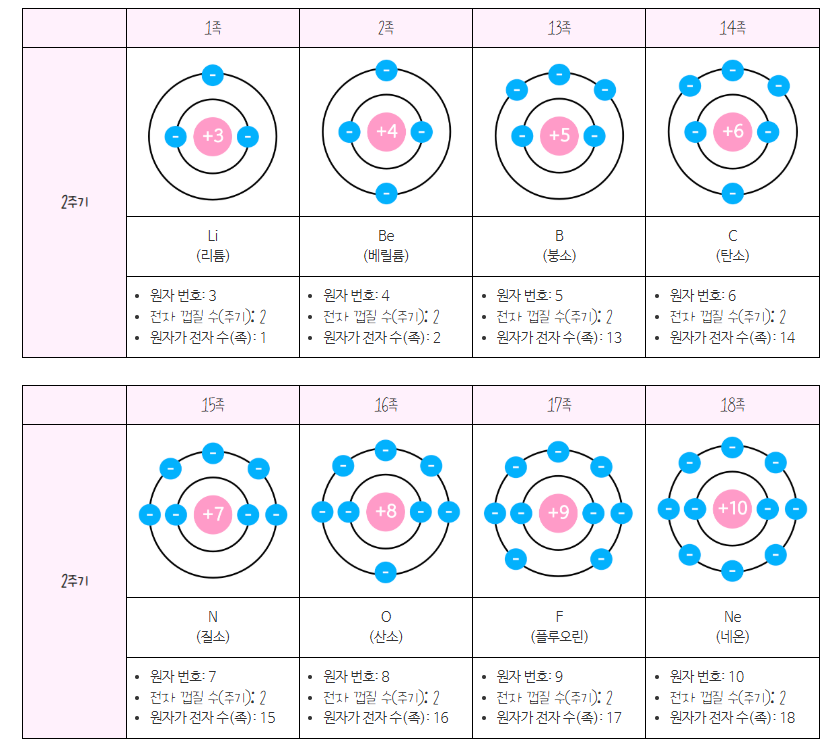
보어의 전자배치는 주로 1주기~3주기까지의 원소들을 나타내는데 쓰인다.
1족에 속한 원소들은 원자가 전자 수가 1개, 2족에 속한 원소들은 원자가 전자수가 2개다.
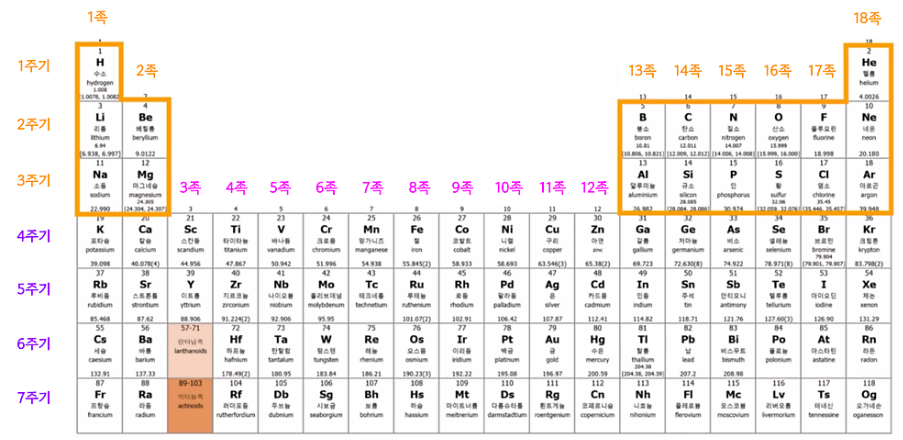
그런데 붕소부터는 3족이 아니라 13족으로 이어진다.
이는 보어의 전자배치로 나타내지 않는 4주기 원소들이 3족 ~12족까지 차지하고 있기 때문이다. 즉, 주기율표를 전체적으로 보았을 때 그 사이에 다른 원소들이 존재하기 때문이다.
이처럼 주기율표에서 주기는 그 원소를 보어의 원자모형으로 나타냈을 때 전자껍질이 몇개가 있는 지를 나타내고, 족은 가장 바깥 껍질에 있는 전자가 몇 개인지를 알려주는데, 11족부터는 숫자가 뒷자리만 생각해서 11족 원소 구리는 가장 바깥 껍질에 있는 전자가가 1개이고, 12족 원소 아연은 2개, 13족원소 붕소는 3개...로 이해한다.
원자가 전자 (valence electron)
원자의 최외각 껍질에 존재하여 화학결합에 참여하는 전자로 원소의 화학적 성질을 주로 결정한다.
① 원자의 가장 바깥껍질(최외각 껍질)에 존재하는 전자
② 화학결합에 참여하는 전자
→ 가장 바깥 전자껍질이 모두 채워져 있지 않으면 화학결합에 참여하여 화학결합을 이루려고 한다.
③ 원소의 화학적 성질을 결정하는데 주된 역할을 한다.
→ 원자가 전자의 수가 같은 원소들은 서로 비슷한 성질을 나타낸다.
→ 분자결합, 고체의 응집메커니즘 등에 기여하며 원자가 등의 화학적 성질을 결정한다.
ex) 원자가 전자의 수가 1개인 1족 원소 리튬과 나트륨의 경우, 전자 1개를 잃고 양이온이 되려는 성질이 있다.
원자가(valence) : 이웃한 동일한 원자 또는 다른 원자와 화학결합을 할 때 가질 수 있는 화학결합의 수
원자의 고유한 성질을 가리키는 값 중 하나
같은 족의 원소들은 같은 값의 원자가를 가진다.
ex) 1족 - 원자가 1, 2족 - 원자가 2, 13족 원자가 - 3, 14족 - 원자가 4, 15족 - 원자가3, 16족 - 원자가 2, 17족 - 원자가 1,
18족 - 원자가 0
⊙ 메테인 분자내 탄소원자는 4개의 수소원자와 결합한다. → 탄소 원자의 원자가는 4
⊙ 암모니아 분자내 질소 원자는 3개의 수소원자와 결합한다. → 질소원자의 원자가는 3
⊙ 물분자내 산소원자는 2개의 수소원자와 결합한다. → 산소원자의 원자가 2
⊙ 메테인, 암모니아, 물 분자내 공통으로 존재하는 수소 원자의 원자가는 1
【최외각 전자 vs 원자가 전자】
최외각 전자는 '최고로 외각에 있는 전자' 즉, 가장 바깥 전자껍질(최외각 껍질)에 존재하는 전자를 말한다. 최외각 전자는 단순히
가장 바깥 전자껍에 있는 전자지만...
원자가 전자는 가장 바깥 전자 껍질(최외각 껍질)에 존재하는 전자이지만 다른 원자와의 화학반응(결합)에 참여하는 전자로 원소의 화학적 성질을 결정하는 역할을 한다.
예를 들어, 산소원자는 첫번째 껍질에 전자 2개, 두번째 껍질에 전자 6개가 채워진 구조이므로 최외각 전자, 즉, 가장 바깥 전자껍질에 있는 전자의 수는 6개이다. 산소원자가 다른 원자와 결합하는 경우 가장 바깥 전자껍질에 있는 최외각 전자 6개가 결합에 참여하게 되는데, 원자가 전자는 최외각 전자 중에서 화학결합에 참여하는 전자를 의미하므로 원자가 전자의 수도 6개이다. 대부분의 원소들은 최외각 전자가 화합결합에 참여하기 때문에 최외각 전자와 원자가 전자가 같다고 본다.
그러나 18족 원소(비활성 기체)들은 최외각 전자와 원자가 전자가 다르다.
18족 원소들 중 헬륨(He)은 최외각 전자가 2개이고, 네온(Ne)부터는 최외각 전자가 8개이다. 18족 원소들은 안정하여 다른 원소들과 결합하지 않으므로 최외각 전자들이 화학결합에 참여하지 않는다. 따라서 이들의 원자가 전자의 수는 0개 이다.
ex) 헬륨(He)의 최외각 전자 2개, 원자가 전자 0개 → 18족 원소들만 '최외각 전자'와
'원자가 전자'가 다름 (원자가 전자 0개)
【 정리 】
① 보어의 원자구조
㉠ 전자는 원자핵 주위의 특정한 궤도(전자껍질)를 따라 운동한다.
㉡ 전자껍질은 에너지 준위( energy level)가 서로 다르다.
㉢ 전자는 안쪽 껍질(에너지가 낮고 안정한 껍질)부터 채워진다.
㉣ 첫번째 껍질에는 전자가 2개까지, 두번째 껍질에은 전자가 8개까지 채워진다.
② 주기율표
㉠ 가로줄 = 주기 / 세로줄 = 족
㉡ 3주기까지의 원소들을 보어의 모형으로 나타냈을 때 같은 주기에 있는 원소들은 전자 껍질의 수가 같다.
㉢ 같은 족에 있는 원소들은 원자가 전자의 수가 같아 비슷한 화학적 성질을 나타낸다.
#보어 #껍질 #원자가전자 #최외각껍질 #원자모형 #주기율표 #주기율 #원자 #분자 #원소 #주기
'위험물 기능장 > 일반화학및유체역학' 카테고리의 다른 글
| 탄화수소 주요 작용기 (1) | 2025.11.02 |
|---|---|
| 탄화수소 명명법(Nomenclature) (0) | 2025.11.02 |
| 위험물의 분류 및 지정수량 (0) | 2025.01.29 |
| 보어의 원자 모형 (주양자수, 에너지 궤도) (2) | 2025.01.28 |
| 위험물의 명명법 (2) | 2025.01.26 |
