1. 보일의 법칙 (Boyle's law)
▣ 보일의 법칙은 기체의 온도가 일정하면 기체의 압력과 부피는 반비례한다는 법칙으로,
영국의 자연철학자, 화학자이자 물리학자인 보일(R. Boyle, 1627-1691)이 1662년에 발견하였다.
▣ 보일의 법칙을 좀 더 엄밀하게 표현하자면, 닫힌계에서 온도와 질량이 일정한 이상기체가 가지는 압력은
그 기체의 부피에 반비례한다는 법칙이다

⊙ 이를 그래프로 나타내면 다음과 같다.

2. 샤를의 법칙 (Charl's law)
▣ 샤를의 법칙은 기체의 부피가 기체의 온도에 비례한다는 법칙으로, 프랑스의 과학자인
샤를 (J. Charles, 1746-1823)이 발견하였다.

▣ 샤를의 법칙은, 좀더 엄밀하게 표현하자면, 기체의 압력이 일정할 때 기체의 부피가 기체의 절대온도에
비례한다는 법칙이며, 수학적으로 표현하면 다음과 같다.

⊙ 이를 그래프로 나타내면 다음과 같다.

3. 보일 - 샤를의 법칙 (Boyle-Charl's law)
▣ 보일·샤를의 법칙은 기체의 부피는 압력에 반비례하고 절대온도에 비례한다는 법칙
으로, 보일의 법칙과 샤를의 법칙을 종합한 것이다.

이를 수식으로 나타내면 다음과 같다.
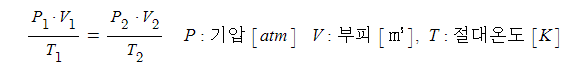
이를 그래프로 나타내면 다음과 같다.

4. 이상기체 상태방정식 ★
▣ 1834년 프랑스의 물리학자이자 공학자였던 클라페롱(B. P. E. Clapeyron, 1799-1864)이
보일의 법칙(Boyle's law)과 샤를의 법칙(Charles's law)를 조합하여 고안하 였다.
이 방정식은 동역학적 이론(kinetic theory)를 이용해서도 유도할 수 있으며,
1856년에 독일 물리학자이자 화학자였던 크뢰니히(K. A. Krönig, 1822-1879)와
1857년에 독일 물리학자이자 수학자였던 클라우지우스(R. J. E. Clausius, 1822-1888)가
서로 독립적으로 발견했다.

이를 수식으로 표현하면 다음과 같다.

【 출제 예상 문제】
1. 실내에서 화재가 발생했을 경우, 처음 실내의 온도가 21 [℃]에서 화재시 실내의 온도가
650 [℃]가 되었다면 이로 인하여 팽창된 공기의 부피는 처음의 약 몇 배가 되는가 ?
[단, 대기압은 공기가 유통하여 화재 전이나 후가 거의 같다고 한다.) ①
① 3 ② 6 ③ 9 ④ 12
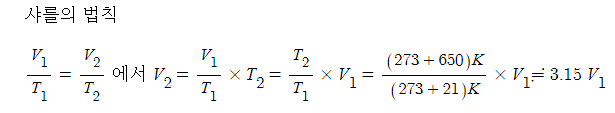
2. 표준상태 11.2[ℓ]의 기체질량이 22[g] 이었다면 이 기체의 분자량은 얼마인가 ? ③
① 22 ② 35 ③ 44 ④56

3. 위험물 탱크에 압력이 0.3[Mpa]이고, 온도가 0[℃]인 가스가 들어 있을 때 화재로 인하
여 100 [℃] 까지 가열되었다면 압력은 약 몇 [Mpa]인가 ? (단, 이상기체로 가정한다) ①
① 0.41 ② 0.52 ③ 0.63 ④ 0.74

'소방설비기사 (전기) > 소방원론' 카테고리의 다른 글
| 유류화재 - 화재론 - 소방학개론 (0) | 2022.10.22 |
|---|---|
| 화재 - 화재론 - 소방원론 (0) | 2022.10.21 |
| 위험물 - 연소론 - 소방원론 (2) | 2022.10.17 |
| 점화원 - 연소론 - 소방원론 (0) | 2022.10.16 |
| 산소 - 연소론 - 소방원론 (2) | 2022.10.15 |
