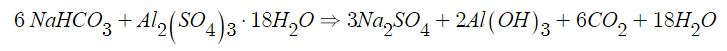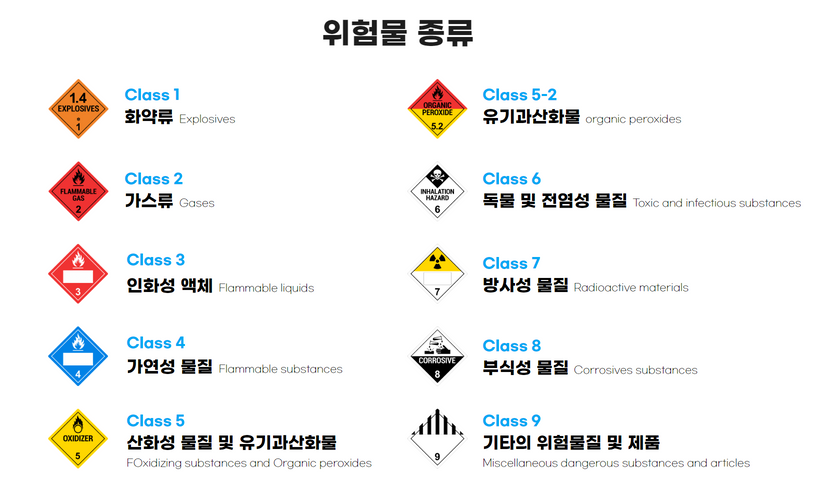
【 위험물의 분류 】
▣ 제1류 위험물 : 산화성 고체
▣ 제2류 위험물 : 가연성 고체
▣ 제3류 위험물 : 자연발화성 물질, 금수성 물질
▣ 제4류 위험물 : 인화성 액체
▣ 제5류 위험물 : 자기연소성 물질
▣ 제6류 위험물 : 산화성 액체
1. 제1류 위험물 (산화성 고체)
▣ 산소공급원이 될 수 있고 형태는 고체이다.
▣ 제1류 위험물은 가연물이 아니므로 가연물과 멀리 하면 된다.
<제1류 위험물의 공통 성질>
◈ 위험물 (물질, 분자) 상태에서는 매우 안정하다.
◈ 화합물 내에 산소를 함유하는 고체 물질이다.
◈ 분해하여 산소를 방출하며, 산소공급원의 기능을 한다.
◈ 그러므로 분해 되지 않도록 취급 · 저장한다.
◈ 가열 · 충격 · 마찰 등 분해를 촉진하는 물질과 접촉을 피한다.
※ 분자식에 반드시 산소가 들어가 있어야 한다.
※ ex) NaClO3 → 열분해 : NaCl + 3/2 O2
① 대부분 무색결정 또는 백색 분말로서 비중이 1보다 크다.
② 대부분 물에 잘 녹는다.
③ 일반적으로 불연성이다.
④ 산소를 많이 함유하고 있는 강산화제이다.
※ 조연성 물질 : 강산화제, 가연성 물질 : 강환원제
⑤ 반응성이 풍부하여 열, 타격, 마찰 또는 분열을 촉진하는 약제와 접촉하여 산소를 발생한다.
[저장 및 취급방법]

◈ 대부분 조해성을 가지므로 습기 등에 주의하여 밀폐 용기에 저장할 것
※ #조해성 : 공기중의 습기에 녹는 것
◈ 통풍이 잘되는 차가운 곳에 저장할 것
◈ 열원이나 산화되기 쉬운 물질 및 화재위험이 있는 곳에서 멀리할 것
◈ 가열, 충격, 마찰 등을 피하고 분해를 촉진하는 약품류와 접촉을 피할 것
◈ 취급시 용기의 파손에 의한 위험물의 누설에 주의할 것
[제1류 위험물의 소화방법]
◈ 대량의 물을 주수하는 냉각소화
※ 분해 온도 이하로 유지하기 위하여
◈ 무기과산화물 (알칼리금속의 과산화물)은 급격히 발열반응하므로 탄산수소염류의 분말소화약제,
건조사에 의한 피복소화
※ 무기물은 금속계통이므로 무기물이 들어 있으면 물과 급격히 반응하므로 물을 소화약제로 사용할 수 없다.
2. 제2류 위험물 (가연성 고체)
※ 가연성 고체이므로 점화원으로 멀리하고 산소 공급원으로 멀리한다.
[제2류 위험물의 공통성질]
◈ 상온에서 고체이고 강환원제로서 비중이 1보다 크다.
◈ 비교적 낮은 온도에서 착화되기 쉬운 가연성 물질이며 연소시 유독가스가 발생하는 것도 있다.
◈ 철분, 마그네슘, 금속분류는 물과 산의 접촉으로 발열한다.
◈ 산화제와의 접촉, 마찰로 인하여 착화되면 급격히 연소한다.
[제2류 위험물의 저장 및 취급방법]
◈ 점화원으로 부터 멀리하고 가열을 피할 것
◈ 산화제와의 접촉을 피할 것
◈ 철분, #마그네슘, 금속분류는 물과의 접촉을 피할 것
◈ 용기등의 파손으로 위험물의 누설에 주의할 것
[제2류 위험물의 소화방법]
◈ 주수에 의한 냉각 소화
◈ 마그네슘, 금속분류는 건조사 피복에 의한 질식소화
3. 제3류 위험물 (자연발화성 물질 및 금수성 물질)
※ 활성금속, 1족 금속, 2족 중 아래 위치 금속
※ 공기중에 습기와도 반응을 한다. 온도 상승에 의한 자연발화한다.
<제3류 위험물의 공통 성질>
◈ 대부분 무기물의 고체이다.
* 발화점 : #황린 34[℃], 대부분 금속인데 황린은 유기물이다.
※ 대부분 고체인데 알킬알루미늄, 알킬리듐은 액체이다.
◈ 자연발화성 물질로서 공기와의 접촉으로 자연발화의 우려가 있다.
◈ 금수성 물질로서 물과 접촉하면 발열 · 발화한다.
<제3류 위험물의 저장 및 취급방법>
◈ 용기의 파손, 부식을 막고 공기와의 접촉을 피할 것
◈ 금수성 물질로서 수분과의 접촉을 피할 것
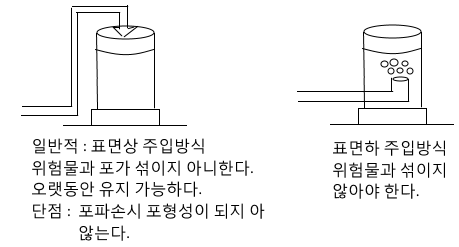
◈ 보호액 속에 저장하는 위험물은 위험물이 보호액 표면에 노출되지 않도록 할 것
◈ 다량을 저장하는 경우에는 소분하여 저장할 것
※ Na, K : 석유속에 저장한다.
황린(P4), 제4류 위험물 이황화탄소(CS2) : 물속에 저장한다.
※ 이황화탄소 : 위험도가 가장 큰 물질
<제3류 위험물의 소화방법>
◈ 건조사, #팽창질석, 팽창진주암을 이용한 질식 소화
※ 주수소화는 절대 엄금
◈ 금속화재용(탄산수소염류) 분말 소화약제에 의한 질식소화가 효과적이다.
4. 제4류 위험물 (인화성 액체)
※ 모든 위험물은 위험등급 1등급, 2등급, 3등급이 있다. 1등급이 가장 위험하다.
※ 인화가 잘되는 물질 : 인화점이 낮다. 증기압이 크다. 비점이 낮다.
※ 1등급 특수인화물 : 지정수량을 부피로 정하며 50[ℓ] 가 지정수량이다.
2등급 제1석유류, 알코올류 : 비수용성보다 수용성이 지정수량이 2배 많다.
* 비수용성이나 수용성은 인화점이 비슷한데 불이 붙고 나서 소화를 할 때 수용성 위험물 소화에는 물을 소화약제로
사용할 수 있어 안전성이 높다고 볼 수 있다.
<제4류 위험물의 공통성질>
◈ 상온에서 액체 이며 인화의 위험이 높다.
◈ 대부분 물보다 가볍고 물에 녹지 않는다.
◈ 증기는 공기보다 무겁다.
(기체의 무게는 분자량으로 따진다 메탄 CH4 16, 에탄 C2H6 30, 공기 29)
◈ 비교적 낮은 착화점을 갖고 있다.
◈ 증기는 공기와 약간만 혼합되어 있어도 연소의 우려가 있다.
※ 폭발범위 하한값이 낮다. 가솔린 1.4 ~ 7.6 인데 대부분 이와 비슷하다.
◈ 용기는 밀전하고 통풍이 잘되는 찬 곳에 저장할 것
◈ 화기 및 #점화원 으로 부터 먼 곳에 저장할 것
◈ 증기 및 액체의 누설에 주의하여 저장할 것
◈ 인화점 이상으로 취급하지 말 것
◈ 정전기의 발생에 주의하여 저장 · 취급할 것
◈ 증기는 높은 곳으로 배출할 것 (굴뚝 4[m] 이상으로 한다)
< 제4류 위험물의 소화방법>
◈ 수용성 위험물
⊙ 초기(소규모) 화재시 : 물분무, 탄산가스, 분말방사에 의한 질식소화
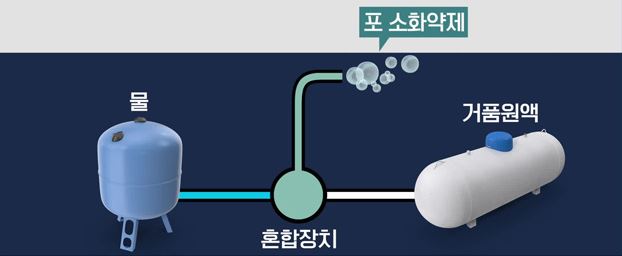
⊙ 대형화재의 경우 : 알코올포 방사에 의한 질식 소화
◈ 비수용성 위험물
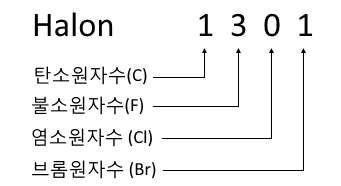
⊙ 초기(소규모) 화재시 : 탄산가스 분말, 할론방사에 의한 질식 소화
⊙ 대형화재의 경우 : 포말 방사에 의한 질식 소화
<제4류 위험물의 구분>
◈ 특수인화물
⊙ 디에틸에테르, #이황화가스
⊙ 1기압에서 발화점이 100 [℃] 이하인 것
⊙ 인화점이 - 20 [℃] 이하이고 비점이 40 [℃] 이하인 것
◈ 제1석유류
⊙ 아세톤, 휘발유
⊙ 1기압에서 인화점 21 [℃] 미만인 것
◈ 알코올류
⊙ 1분자를 구성하는 탄소원자수가 1~개 까지인 포화1가 #알코올 (변성알코올 포함)
※ 알칸, 알켄, #알킬 중에 알킬류...
알킬 R : Cn H2n+1 ⇒ 알코올은 알킬과 OH 결합 : R + OH
분자수가 많아지면 많아질수록 인화위험은 적다
CH3 OH - 알코올 램프용 인화위험이 가장 크다.
C2H5 OH - 술의 원료
C3H7 OH -
변성알코올
※ 알코올류는 위험도가 제1석유류와 비슷하다. 그래서 위치를 1석유류의 바로 뒤에 둔다.
◈ 제2석유류
⊙ 등유, 경유
⊙ 1기압에서 #인화점 21 [℃] 이상, 70 [℃] 미만인 것
◈ 제3석유류
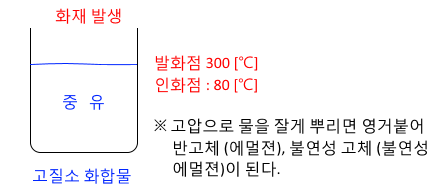
⊙ 중유, 클래오소오드유
⊙ 1기압에서 인화점 70[℃] 이상, 200 [℃] 미만인 것
◈ 제4석유류
⊙ 기계유, 실린더유
⊙ 1기압에서 인화점 200 [℃] 이상, 250 [℃] 미만인 것
◈ 동 · 식물유류
⊙ 동물의 지육 또는 식물의 종자나 과육으로 부터 추출한 것으로서
1기압에서 인화점이 250 [℃] 미만인 것
※ 제4류 위험물이 될려면 인화점이 250 [℃] 미만이어야 한다.
⊙ 지정수량 10,000[ℓ] : 위험도가 가장 낮다.
⊙ 탄소수가 많으면 많을 수록 인화위험은 적고 발화위험은 크다.
※ 동식물유류는 분자의 탄소수가 커서 위험도를 발화위험도를 기준으로 한다.
따라서 이 때의 위험도 기준을 요오드 값으로 기준으로 한다.
[요오드 값] - 옥소값
⊙ 정의 : 기름 100[g]에 부가도는 요오드의 g수
※ 2중결합이나 3중 결합을 하는 물질의 경우 다른 물질을 첨가하면
그 물질과 바로 결합하는 것으로 첨가물, 부가물이라고 한다.
※ 동·식물유 100[g]에 요오드를 넣었을 때, 최대 녹을 수 있는 요오드 [g] 수
* 동·식물유류는 불포화지방으로 이중결합, 3중결합으로 되어 있다.
※ #불포화도 가 크면 클수록 반응을 잘하고 요오드값이 커진다.
※ 들기름이 참기름보다 불포화도가 커서 반응을 잘한다. 들기름이 참기름 보다 이중결합, 3중결합이 많고
이는 불포화도가 커셔 요오드값이 크고 공기중에 놓으면 들기름이 참기름보다 공기중의 산소와 반응을 잘해
자연발화가 잘 될 것이다. 분자가 클수록 산소와 결합하여 산화열을 축적하여 자연발화가 잘된다.
[동 · 식물유류의 구분]
⊙ 건성유 : 요요드값 130 이상
(해바라기기름, 동백유, 아마인유, 들기름, 정어리기름)
⊙ 반건성유 : #요오드 값 100 이상 ~ 130 미만 : 참기름
⊙ 불건성유 : 요오드값 100 미만
5. 제5류 위험물 (자기연소성, #자기반응성, 내부연소성 물질)
▣ #가연물 이면서 산소공급원을 함께 보유하고 있는 물질
▣ 2가지 성분을 함께 가지고 있는 반응이 매우 빠르다.
▣ 제5류 위험물은 #폭발성 물질이다. 가연물 + 산소공급원
▣ 소화방법은 질식 소화방법을 쓸 수 없다. 스스로 산소공급원이기 때문이다.
< 제5류 위험물의 공통성질 >
◈ 가연성이면서 분자 내에 산소를 함유하고 있는 자기연소성 물질이다.
◈ 유기물질로 연소속도가 매우 빨라 폭발적으로 연소한다.
◈ 가열 · 충격 · 마찰 등에 의하여 폭발의 위험이 있다.
◈ 공기 중에서 장시간 방치하면 자연발화를 일으킬 수 있다.
※ 햇빛을 받으면 열을 축적하여 자연발화할 위험이 있다.
※ 자연발화를 막기 위해 물에 적시거나 알코올 등에 적시어 저장한다.
< 제5류 위험물의 저장 및 취급방법>
◈ 화재시 소화가 어려우므로 소분하여 저장할 것
◈ #가열 , 충격, #마찰 을 피하고 화기 및 점화원으로 부터 멀리할 것
◈ 용기의 파손 및 균열에 주의하고 통풍이 잘되는 냉암소에 저장할 것
◈ 용기는 밀전 · 밀봉하고 운반용기 및 포장외부에는 "화기엄금", "충격주의" 등의 주의사항을 게시할 것
<제5류 위험물의 소화방법>
◈ 초기소화에는 주수에 의한 냉각소화
6. 제6류 위험물 (산화성 액체)
※ 물성이 액체이면 제6류 위험물이고 #고체 이면 제1류 위험물이다.
※ 특성 등은 제1류 위험물과 비슷하다.
※ #화합물 상태에서는 위험성이 없으나 분해되면 위험하다.
<제6류 위험물의 공통성질 >
◈ 산화성 액체로 비중이 1보다 크며 물에 잘 녹는다.
◈ 불연성이지만 분자내에 산소를 많이 함유하고 있어 다른 물질의 연소를 돕는 조연성 물질이다.
◈ 부식성이 강하며 증기는 유독하다.
◈ 가연물 및 분해를 촉진하는 약품과 접촉시 분해되어 폭발한다.
< 제6류 위험물의 저장 및 취급방법>
◈ 가연물, 유기물 및 산화제와의 접촉을 피할 것
◈ 물과 접촉시 발열하므로 접촉에 주의할 것
※ 강한 #산화제 이다. 물과 만나면 발열반응을 한다.
강산화제는 피부에 닿으면 화상을 입는다.
※ 액성이 강한 산성물질은 플라스틱을 녹이고 금속을 부식시킨다.
◈ 저장용기는 #내산성 용기를 사용하여 밀전하여 누설에 주의할 것
◈ 증기는 #유독 하므로 #보호구 를 착용할 것
※ 제6류 위험물에는 과산화수소 (H2O2)는 농도가 36 [wt%]이 넘으면 위험물이 된다.
* H2O2 → H2O + 1/2 O2 과산화수소는 분해가 잘되는데 액체가 기체로 변하면 부피가 매우 커지므로
농도가 위험물의 기준치를 넘게 되어 매우 위험물질이 된다.
* 따라서 모든 위험물 저장용기는 밀전, 밀봉을 하나 유일하게 구멍 뚫린 마개를 사용하는 위험물질이
#과산화수소 이다.
< 제6류 #위험물 의 소화방법 >
◈ 소량일 때는 대량의 물로 희석소화
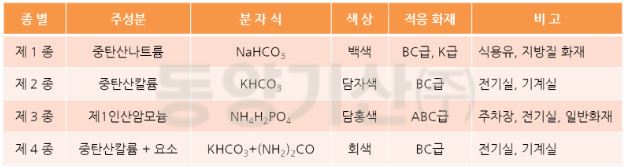
◈ 대량일 대는 주수소화가 곤란하므로 #건조사 , #인산염류 의 #분말 로 #질식소화
7. #특수가연물
※ 특수가연물은 위험물에 속하지 않고 일반 가연물에 포함된다.
※ 가연성 액체중에서는 인화점이 250 [℃] 이상인 물질을 말한다.
'소방설비기사 (전기) > 소방원론' 카테고리의 다른 글
| 소화약제 출제 예상 문제 (0) | 2023.04.20 |
|---|---|
| CDC 소화약제 및 금속화재용 분말 소화약제 (2) | 2023.04.19 |
| 충전비와 이산화탄소(CO2) 약제 계산식 (0) | 2023.04.19 |
| 이산화탄소 · 분말 · 할로겐 화합물 소화약제 (2) | 2023.04.18 |
| 물 · 포 소화약제 : 소화약제의 종류 (0) | 2023.04.18 |